Синдром раздраженного кишечника причины, симтомы и таблетки для лечения
Наверное, на планете Земля не найдется такого «счастливчика», который ни разу не произнес бы эту фразу. Причем – с полным на то основанием.
Читать полностью
Е.Б.Авалуева1, Т.В.Адашева2, А.Р.Бабаева3, Е.Г.Бурдина4, Н.В.Киреева5, Л.Г.Ленская6, М.А.Осадчук5, И.Г.Пахомова1, Л.И.Попова7, Е.И.Ткаченко1, Ю.П.Успенский8, Ю.Г.Шварц9, А.А.Мысливец10, Е.Н.Андрианова10
1ГБОУ ВПО Северо-Западный государственный медицинский университет им. И.И.Мечникова Минздрава России, Санкт-Петербург; 2ГБОУ ВПО МГМСУ им. А.И.Евдокимова Минздрава России;
3ГБОУ ВПО Волгоградский государственный медицинский университет Минздрава России;
4ФГБУ Поликлиника №3 Управления делами Президента Российской Федерации, Москва;
5ГБОУ ВПО Первый МГМУ им. И.М.Сеченова Минздрава России;
6ОГАУЗ Томская областная клиническая больница;
7ООО Госпиталь «ОрКли», Санкт-Петербург;
8Городской центр заболеваний кишечника и эндоэкологии желудочно-кишечного тракта, Санкт-Петербург;
9ГБОУ ВПО Саратовский государственный медицинский университет им. В.И.Разумовского Минздрава России;
10ООО НПФ «Материа Медика Холдинг», Москва
Его частота в западных странах составляет около 20%; до 40% больных приходится на наиболее активный трудоспособный возраст — 30–50 лет [2–4]. Женщины болеют в 2 раза чаще мужчин [4]. Качество жизни и трудоспособность лиц, страдающих СРК, снижаются, и ведут они себя зачастую как больные с тяжелым органическим заболеванием при удовлетворительном общем состоянии и отсутствии признаков прогрессирования болезни при динамическом наблюдении [9].
Патофизиологическую основу СРК составляют расстройства моторной и чувствительной функции желудочно-кишечного тракта (ЖКТ), субклинические воспалительные изменения, нарушенный кишечный микробиом и ассоциированные с висцеральными психофизиологические расстройства [1, 3–6]. Условием формирования висцеральной гиперчувствительности является воздействие «сенсибилизирующих» факторов, среди которых рассматриваются кишечные инфекции, психосоциальный стресс, физическая травма, так или иначе ассоциированные с абдоминальной болью [1, 7–9].
В последние годы показано, что пусковым звеном в дебюте СРК, как правило, является стресс, вызывающий появление чрезмерных эмоций. В условиях стресса происходит активация нейропептида (субстанции Р), способствующего появлению воспалительных изменений слизистой оболочки толстой кишки (СОТК) минимального характера. Считается, что воспаление играет основную роль в формировании постинфекционного СРК (ПИ-СРК). Доказано, что воспалительный процесс после перенесенной кишечной инфекции может персистировать в течение длительного времени, локализуясь в СОТК и соседних лимфатических узлах. В патогенезе воспаления при ПИ-СРК существенное значение принадлежит гиперплазии и гиперфункции тучных клеток, активации моноцитов, индуцирующих развитие иммунного воспаления [10]. У пациентов с СРК определяется увеличение экспрессии в СОТК индуцибельной NO-синтазы, интерлейкина-1, что также способно инициировать воспалительный процесс. Установлено, что развитие любого типа СРК ассоциируется с гиперплазией энтерохромаффинных клеток, продуцирующих серотонин, мелатонин, а также с высокой экспрессией пептида YY, инфильтрацией СОТК разными клетками воспаления (лимфоциты, макрофаги, плазмоциты). При этом активность воспалительного процесса в СОТК у пациентов с СРК подтверждалась обнаружением высокого количества клеток, иммунопозитивных к основному маркеру воспаления — кальпротектину [11].
Клиническими проявлениями висцеральной гиперчувствительности являются симптомы гипералгезии и аллодинии (расстройство функции, вызываемое болевыми воздействиями). Доказано, что при СРК нарушен процесс нисходящего подавления восприятия боли, т.е. имеется центральная антиноцицептивная дисфункция, болевой порог в 3 раза меньше, чем у здоровых лиц [3]. Висцеральная гипералгезия, которая расценивается как маркер СРК, проявляется в виде повышенной чувствительности к болевым стимулам и ощущением боли, которое вызвано неболевыми стимулами, симптомы СРК, а именно: метеоризм, нарушениемоторики, транзита и акта дефекации, рассматриваются как вторичные, вызванные синдромом боли.
Специфической симптоматики СРК не существует [2, 3]. Отличительная особенность СРК — многообразие жалоб — как гастроэнтерологических, так и негастроэнтерологических (кардиалгических, респираторных, астенических, цефалгических и т.д.), а также наличие психоневрологических расстройств [12]. Характерным для СРК является наличие абдоминальной боли в сочетании с диареей или запорами [3, 4, 13]. Боль в животе может быть разной интенсивности и локализуется, как правило, внизу живота, хотя может отмечаться и в других его отделах. Она часто усиливается после нарушения диеты, при всплеске эмоций, на фоне нервного и физического переутомления. Боль уменьшается обычно после акта дефекации или отхождения газов и не беспокоит в ночное время. Наряду с болями пациенты нередко отмечают изменения частоты стула (более 3 раз в день и менее 3 раз в неделю), формы и консистенции кала, появление слизи в кале. Типичным считается длительное течение заболевания и резистентность к лечению гастроэнтерологическими средствами [2, 4, 7, 14].
Продолжающиеся до настоящего времени попытки разработать эффективную схему терапии СРК с пролонгированным действием не дали результата ни для одного варианта течения заболевания. Очевидно, это связано с тем, что проблема поиска и объективной оценки эффективности того или иного препарата затруднена из-за сложности и малоизученности патофизиологии СРК и достаточно высокого эффекта плацебо в этой группе пациентов [2, 4, 13].
Новым подходом в терапии СРК является применение комплексного релиз-активного препарата Колофорт, созданного компанией НПФ «Материа Медика Холдинг» на основе антител к человеческому фактору некроза опухоли a (анти-ФНО-a), мозгоспецифическому белку S-100 (анти-S100) и гистамину (анти-Н). Сочетание трех активных компонентов позволяет воздействовать на центральные и периферические звенья патогенеза функциональных нарушений кишечника, в том числе висцеральной гиперчувствительности, способствует уменьшению выраженности абдоминального болевого синдрома и восстановлению нарушенной моторики ЖКТ. Проведенные ранее доклинические и клинические исследования показали эффективность и безопасность Колофорта и его компонентов в лечении гастроинтестинальной патологии воспалительного и функционального генеза, а также в купировании соматоформных дисфункций и психоневрологических расстройств на фоне соматических и неврологических заболеваний [15–18].
Безусловный интерес для многих специалистов представляют результаты многоцентрового рандомизированного клинического исследования, которое проводилось с целью показать клиническую эффективность и безопасность Колофорта при лечении пациентов с СРК в условиях двойного слепого плацебо-контроля.
В исследовании приняли участие 128 пациентов (33 мужчины и 95 женщин) 19–59 лет (средний возраст 36,8±12,1 года), причем большая часть участников была в наиболее активном и трудоспособном возрасте от 25 до 45 лет, что типично для СРК. Все пациенты имели клинические симптомы, характерные для СРК, этот диагноз был верифицирован в соответствии с Римскими критериями III (2006 г.) и исключал наличие структурных или биохимических отклонений со стороны кишечника, что было подтверждено комплексным инструментальным и лабораторным обследованием. В исследовании принимали участие пациенты с тремя вариантами (субтипами) СРК. В соответствии с Римскими критериями III и Бристольской шкалой формы кала пациенты подгруппы СРК с преобладанием диареи имели кашицеобразный (6-й тип) или водянистый (7-й тип) кал при более 25% из общего количества опорожнений кишечника, однако допускалось наличие твердого (1-й тип) или комковатого (2-й тип) кала при менее 25% из общего числа опорожнений кишечника. Участники исследования подгруппы СРК с преобладанием запора имели твердый (1-й тип) или комковатый (2-й тип) кал при более 25% из общего количества опорожнений кишечника, однако допускалось наличие кашицеобразного (6-й тип) или водянистого (7-й тип) кала при менее 25% из общего числа опорожнений. У пациентов со смешанным типом СРК твердый или комковатый кал чередовался с кашицеобразным или водянистым при 25% и более из общего количества опорожнений кишечника. Пациенты с возможным 4-м «неклассифицированным» типом СРК, при котором отклонения консистенции кала имеют недостаточную выраженность для указанных типов, не участвовали в исследовании.
Больной не включался в исследование при наличии декомпенсированных хронических заболеваний, дебюте симптомов СРК после 50 лет, обнаружении патогенной микрофлоры в кишечнике на момент включения в исследование, любых лапароскопических и лапаротомических хирургических вмешательств в анамнезе, прочих заболеваний ЖКТ, включая целиакию, онкологических заболеваний, активного туберкулеза, вирусного гепатита B или C, ВИЧ-инфекции.
В соответствии с современными рекомендациями по оценке эффективности препаратов для лечения СРК в качестве первичного критерия анализировали изменение интенсивности абдоминальной боли (биологического маркера СРК) [6, 19]. Первичной конечной точкой исследования была доля пациентов со снижением на 30% и более выраженности боли/дискомфорта через 4 и 12 нед лечения. В качестве вторичных критериев эффективности оценивали:
Наиболее объективным инструментом оценки тяжести абдоминальной боли/дискомфорта и ее исходов на фоне терапии являются предоставляемые пациентом данные (Patient Reported Outcome), которые выражаются в условных единицах/баллах с помощью валидированных шкал. Один из таких инструментов, который применяли в рамках настоящего исследования, — 11-балльная визуальная аналоговая шкала (ВАШ), оценивающая тяжесть боли от 0 до 10 (Numeric Rating Scale). Для оценки клинических проявлений СРК и их динамики на фоне терапии помимо ВАШ использовали следующие шкалы и опросники: ВАШ оценки выраженности симптомов СРК (Visual Analog Scale — Irritable Bowel Syndrome — VAS-IBS), индекс висцеральной чувствительности (Visceral Sensitivity Index — VSI), госпитальную шкалу тревоги и депрессии (Hospital Anxiety and Depression Scale — HADS), опросник качества жизни при СРК (Irritable Bowel Syndrome — Quality of Life — IBS-QoL).
На этапе скрининга проводили сбор анамнеза и жалоб, физикальные, лабораторные и инструментальные обследования, с помощью которых исключали другие помимо СРК причины патологической симптоматики. Инструментальные и лабораторные обследования включали колоноскопию, по показаниям − биопсию и гистоморфологические исследования, ультразвуковое исследование органов брюшной полости и малого таза, электрокардиографию в 12 отведениях, общеклинические анализы крови и мочи, биохимический анализ сыворотки крови с определением С-реактивного белка, общего белка, креатинина, глюкозы, аланинаминотрансферазы, аспартатаминотрансферазы, амилазы, исследования кала с оценкой физико-химических (консистенция, цвет, запах, реакция, билирубин, стеркобилин) и микроскопических показателей (мышечные волокна, нейтральный жир, жирные кислоты, мыла, клетчатка, лейкоциты, эритроциты и другие показатели), анализ на дизентерийную группу и яйца гельминтов.
В течение 2-недельного скринингового наблюдения (1 и 2-й визиты) пациенты вели дневники, что позволило наряду с анкетированием и тестированием оценить исходную выраженность основных симптомов СРК. После включения в исследование (3-й визит, 0-й день) пациенты рандомизировались в одну из двух групп. Пациенты 1-й группы (группа Колофорта) получали исследуемый препарат по 2 таблетки 2 раза в сутки в течение 12 нед, пациенты 2-й группы (группа плацебо) получали плацебо по схеме приема Колофорта.
В течение последующего периода лечения пациенты совершали 5 визитов (4–8-й визиты) в медицинский центр, в ходе которых оценивалось состояние, проводились объективные и лабораторные обследования, тестирование и анкетирование, регистрировались сопутствующая терапия, возможные нежелательные явления, комплаентность. В ходе всего исследования пациенты продолжали вести дневник, где фиксировали состояние, возможные патологические симптомы, нежелательные явления, прием исследуемого и сопутствующих лекарственных препаратов.
Подгруппы с СРК с преобладанием диареи (n=48; 42%) или запора (n=50; 44%) были равными по численности, значительно меньшее число больных имели смешанный вариант СРК (n=16; 14%). Сопутствующие заболевания зарегистрированы у 55% участников исследования, в том числе болезни органов кровообращения (20%, включая артериальную гипертензию, которая выявлялась у 12% пациентов), воспалительные и невоспалительные заболевания органов мочеполовой системы (25%), позвоночника/суставов/мягких тканей (16%), респираторной (15%) и эндокринной (8%) системы. Патология нервной системы (9%) регистрировалась преимущественно в виде астеновегетативных и неврозоподобных расстройств, типичных для пациентов с СРК. В качестве сопутствующей терапии 7% больных получали антигипертензивную терапию, 14% женщин-участниц детородного возраста применяли пероральные комбинированные препараты с целью контрацепции. В ходе исследования использовались разные препараты для лечения острых респираторных инфекций, включая противовирусные средства (4%), редко — лекарственные средства других групп (статины, сахароснижающие препараты и др.).
В течение всего исследования пациенты могли получать симптоматическую терапию СРК (Смекта®/Гутталакс®/Но-шпа® − при наличии показаний) и препараты для лечения сопутствующей патологии за исключением запрещенных препаратов, которые включали средства, воздействующие на ЖКТ (слабительные, прокинетики, спазмолитики, агонисты опиатных рецепторов); ветрогонные средства, антибиотики, нестероидные и стероидные противовоспалительные препараты, психотропные препараты (антидепрессанты, анксиолитики, антипсихотические средства, препараты лития и седативные средства), пробиотики и прочие препараты, в инструкции по медицинскому применению которых указано влияние на функциональное состояние кишечника.
Статистическая обработка полученных данных проводилась с помощью статистического пакета SAS 9,3. Из элементов описательной статистики определялись: среднее арифметическое значение, стандартное отклонение, количество наблюдений — для количественных признаков; доли и проценты пациентов с тем или иным показателем — для качественных признаков. Использовались методы параметрической (для непрерывных и интервальных переменных) и непараметрической (частотный анализ по категориальным переменным) статистики.
Исходная средняя интенсивность боли на визитескрининга была 6,1±1,7 балла у пациентов группы Колофорта и чуть ниже (5,6±1,5 балла) у пациентов группы плацебо. Несмотря на применение разрешенных лекарственных препаратов для облегчения симптомов заболевания на протяжении 2 нед наблюдения, интенсивность абдоминальной боли к 3-му визиту (0-й день) практически не изменилась, оставаясь более выраженной в группе Колофорта (6,0±1,7 балла против 5,2±1,6 балла в группе плацебо).
Снижение интенсивности боли на 30% и более по сравнению с исходным состоянием было зарегистрировано у 56% пациентов через 4 нед и 90% больных через 12 нед лечения Колофортом, что, по данным частотного анализа, значимо превосходило (c 2(1)=8,7; p=0,003) результаты в группе плацебо (67%). Снижение интенсивности болевого синдрома произошло в среднем более чем на 50%.
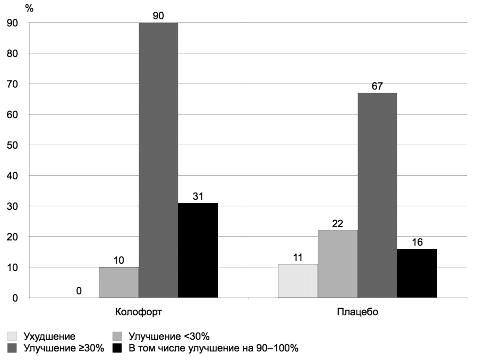
Примерно у 1/3 (31%) участников исследования абдоминальная боль практически полностью купировалась к окончанию периода лечения (снижение интенсивности на 90–100%); в группе плацебо таких больных было в 2 раза меньше (16%). Существенное уменьшение абдоминальной боли регистрировалось у пациентов, ответивших на терапию Колофортом, более 50% длительности периода наблюдения. Кроме того, отмечено, что на фоне лечения Колофортом у всех участников произошло улучшение по основному симптому заболевания, а в группе плацебо у 11% больных зарегистрировано ухудшение, интенсивность болевого синдрома через 12 нед выросла (рис. 1).
Рис. 1. Распределение пациентов по динамике абдоминальной боли через 12 нед лечения.
Выраженность и динамика абдоминальной боли у пациентов группы Колофорта не зависела от приема Но-шпы, разрешенной для купирования спастических болей в животе. Если исходная частота ее применения была 8,0±8,7 раза за 2 нед периода наблюдения, то к окончанию терапии — в 4 раза и более ниже (1,8±3,6 раза за 2 нед; ANOVA Repeated Measures: F(3/333)=3,04; p=0,03).
Таким образом, лечение Колофортом устраняло моторную и рецептивную висцеральную дисфункцию кишечника и гипералгезию за счет влияния на центральные и периферические механизмы формирования абдоминальной боли, значимо снижало ее выраженность и уменьшало потребность в анальгетической (антиспастической/спазмолитической) терапии. Выраженный анальгетический эффект развивался постепенно и отмечался у 100% больных.
Терапевтическое действие Колофорта проявлялось положительным влиянием на паттерн стула (форму и частоту) у пациентов с разными вариантами СРК.
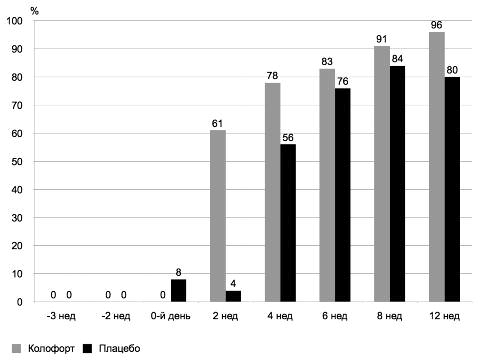
У 13% пациентов группы Колофорта с СРК с преобладанием диареи исходно был 7-й (водянистый), у 87% − 6-й (кашицеобразный) тип стула при 100% опорожнений кишечника. Уже через 2 нед лечения Колофортом улучшение консистенции/формы стула до 5-го типа произошло у 61% пациентов. В группе плацебо, напротив, у 60% участников стул оставался 6-го типа. В результате 3-месячного курса терапии 96% пациентов группы Колофорта имели 5-й тип стула и ниже (против 72% группы плацебо; c 2(1)=5,5; p=0,02); в том числе почти 1/2 пациентов имели нормальный тип стула (4-й — у 35%; 3-й − у 13%); при этом частота стула снизилась с 3 раз и более до 1–2 раз за сутки (рис. 2).
Рис. 2. Динамика долей пациентов с улучшением стула до 5-го типа и менее по Бристольской шкале
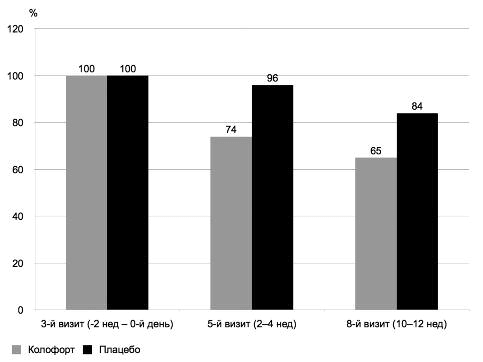
Положительные изменения консистенции/формы стула были сопряжены именно с терапевтическим влиянием Колофорта, а потребность пациентов в применении разрешенной Смекты уменьшалась на 30% в первые 2 нед лечения. Итогом 12-недельного применения Колофорта было 70% снижение необходимости применения средства для облегчения диареи (рис. 3).
Рис. 3. Доля пациентов, принимавших препарат Смекта®.
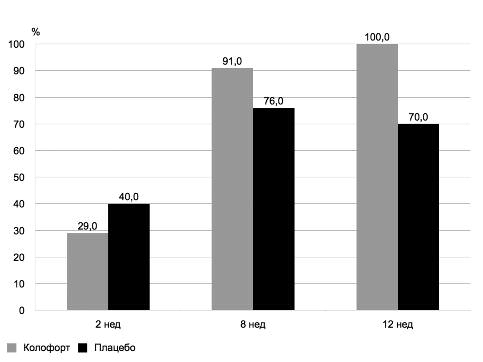
Уменьшение интенсивности абдоминальной боли у пациентов подгруппы СРК с преобладанием диареи примерно на 25% происходило через 2 нед лечения Колофортом и более чем на 50% − через месяц. Начиная со 2-го месяца, анальгетический эффект препаратанарастал и достигал более 70%. При этом снижение интенсивности абдоминального болевого синдрома на 30% и более отмечалось у 100% больных с положительной динамикой формы стула по Бристольской шкале, что существенно превышало эффект плацебо терапии (c 2(1)=7,7; p=0,006). Таким образом, параллельно с восстановлением паттерна стула у 96% больных уменьшение тяжести болевого синдрома имело место у 100% пациентов подгруппы СРК с преобладанием диареи (рис. 4).
Рис. 4. Доли пациентов с одновременным снижением интенсивности абдоминальной боли и улучшением паттерна стула у пациентов с СРК с преобладанием диареи.
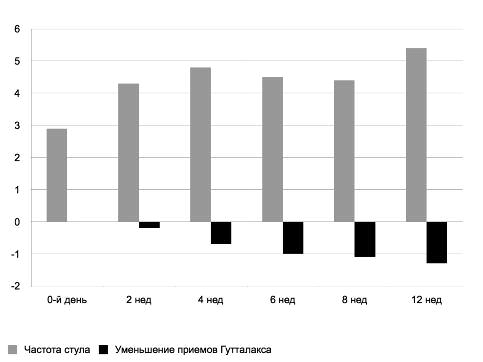
Эффект Колофорта у участников подгруппы СРК с преобладанием запоров также проявлялся в первые 2 нед лечения − средняя частота стула от исходных 1–2 раз в неделю (без применения слабительных средств) и 2,9±1,5 раза в неделю (на фоне применения Гутталакса) возросла до 4,3±2,0 раза за 7 дней. Всего за 12 нед терапии частота актов дефекации увеличилась на 2,5±1,7 раза за неделю, составив в среднем 5,4±2,1 раза за 7 дней. Доля пациентов, у которых произошло увеличение частоты стула на 1 раз и более в неделю, составила 69% и не зависела от приема Гутталакса. За первые 2 нед кратность его применения снизилась почти в 2 раза, а через 3 мес лечения Колофортом — более чем в 5 раз. К окончанию терапии лишь третья часть пациентов нуждалась в редком (1 раз в 2 нед) применении Гутталакса (рис. 5).
Рис. 5. Динамика частоты стула и приемов Гутталакса у пациентов с СРК с преобладанием запоров, лечившихся Колофортом.
Одновременно с улучшением паттерна стула при этом варианте СРК, т.е., начиная с первых недель применения, проявлялось анальгетическое действие Колофорта. Воздействуя на причину и патогенез формирования болевого синдрома, лечение оказывало выраженный анальгетический эффект и приводило к увеличению частоты стула при снижении потребности в симптоматической терапии у 84% больных подгруппы СРК с преобладанием запоров (рис. 6).
Рис. 6. Динамика абдоминальной боли у пациентов с СРК с преобладанием запоров.
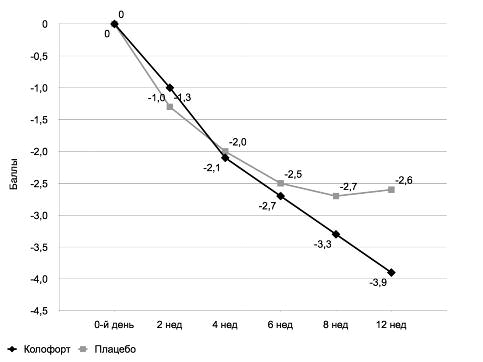
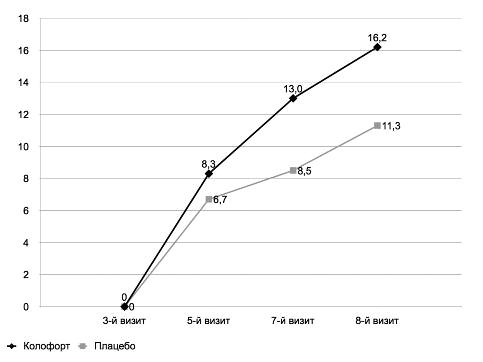
Значимое улучшение паттерна стула в подгруппах СРК с превалированием диареи/запоров, свидетельствующее о восстановление моторно-эвакуаторной функции ЖКТ на фоне лечения Колофортом, подтверждалось результатами анализа данных, полученных с помощью шкалы VAS-IBS. Суммарный балл VAS-IBS, который позволяет оценить влияние препарата как на симптомы со стороны кишечника, так и на психологическое состояние пациента, значимо снижался от исходных 32,2±9,3 до 14,0±10,7 балла (F(2/224)=43,4; p<0,0001), существенно превышая действие плацебо терапии (F(1/112)=4,3; p=0,04); рис. 7.
Рис. 7. Динамика суммарного балла шкалы VAS-IBS в процессе лечения.
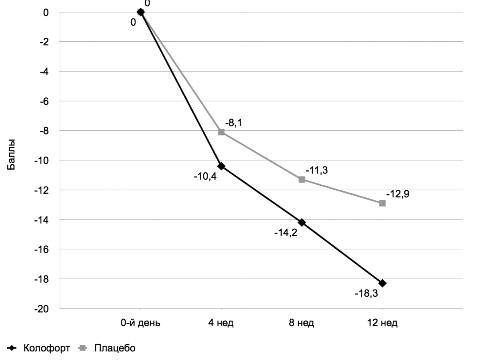
Следует отметить, что положительная динамика в виде снижения выраженности основных клинических симптомов СРК прогрессивно нарастала в течение всех 12 нед применения Колофорта и к окончанию периода лечения «не выходила на плато», что может свидетельствовать о целесообразности продления курса терапии для достижения максимального эффекта у 100% больных.
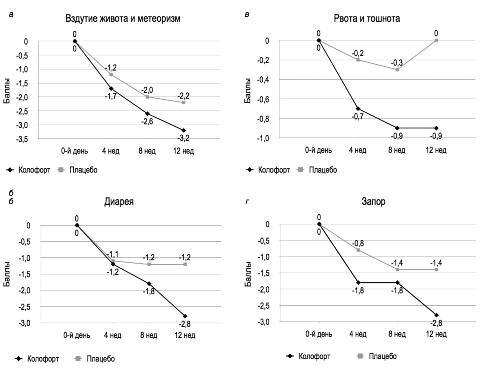
Балл выраженности интестинальной симптоматики также значимо снижался (F(2/224)=38,68; p<0,0001) и превалировал над эффектом плацебо (F(1/112)=4,29; p=0,041). Лечение Колофортом оказывало существенное воздействие на все симптомы со стороны кишечника: явления дискомфорта и вздутия живота, тошноты и рвоты, диареи и запоров (рис. 8); снижался процент пациентов, которые имели императивные позывы на дефекацию и чувство неполного опорожнения кишечника.
Рис. 8. Динамика симптомов со стороны кишечника по данным шкалы VAS-IBS: а — вздутие живота и метеоризм; б — диарея; в — рвота и тошнота; г — запор.
Отмеченные позитивные сдвиги были сопряжены с корригирующим воздействием препарата на висцеральную чувствительность, о чем свидетельствовало значимое изменение индекса VSI (Visceral Sensitivity Index) на фоне терапии Колофортом (F(2/224)=7,5; p<0,0001); рис. 9.
Рис. 9. Динамика индекса висцеральной чувствительности в процессе лечения.
Таким образом, лечение Колофортом оказывало корригирующее воздействие на проявления ноцицептивной дисфункции, висцеральной чувствительности и гипералгезии, лежащие в основе формирования, прогрессирования и клинической манифестации СРК.
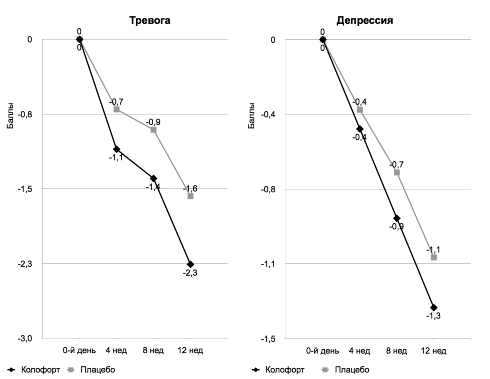
Центральные эффекты Колофорта проявлялись анксиолитическим (ANOVA: F(2/220)=10,27; p<0,0001) и антидепрессивным (F(2/220)=7,50; p=0,0007) действием (рис. 10), что играет очень важную роль в лечении пациентов с СРК.
Рис. 10. Динамика выраженности тревоги и депрессии по шкале HADS в процессе лечения.
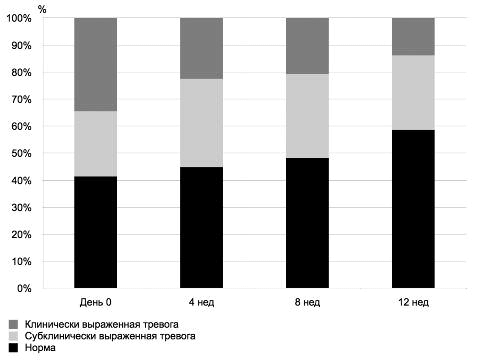
Исходно 1/3 (34%) пациентов группы Колофорта имела клинически значимую тревогу, у 1/4 участников отмечалась субклинически/клинически выраженная депрессия. В процессе терапии значительно увеличился процент пациентов с отсутствием тревожных расстройств и депрессии, а доля больных с субклинически/клинически значимой тревогой/депрессией снизилась (рис. 11).
Рис. 11. Доли пациентов в группе Колофорта с разной степенью выраженности тревоги в процессе лечения.
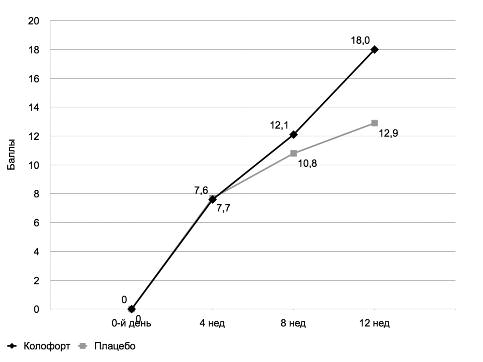
Описанные положительные изменения, которые происходили при лечении Колофортом, включая значимое снижение или полное отсутствие абдоминального болевого синдрома, улучшение либо восстановление многочисленных интестинальных нарушений в сочетании с коррекцией психо-эмоциональных расстройств, позитивно отразились на качестве жизни участников исследования. Оценка с помощью шкалы IBS-QoL, разработанной специально для пациентов с СРК и позволяющей оценить влияние терапии на разные стороны физического и психического здоровья пациента, показала прогрессивно нарастающий прирост суммарного балла, который в итоге увеличился в среднем на 16,2 (рис. 12).
Рис. 12. Изменение качества жизни по шкале IBS-QoL в процессе лечения.
Дисперсионный анализ для повторных измерений подтвердил достоверное улучшение показателя качества жизни к окончанию терапии (фактор «визит»: F(2/224)=30,75; p<0,0001).
Последовательный анализ каждого пункта этого опросника показал позитивные оценки пациентов к окончанию терапии, которые стали следствием того, что применение Колофорта значимо снизило негативное воздействие проблем, связанных с болезнью. Большинство пациентов отмечали выраженное уменьшение чувства дискомфорта, под которым понимают неприятные ощущения в животе, вызванные усиленной перистальтикой, метеоризмом, вздутием, спастическими явлениями. В результате того, что жизнь «перестала вращаться вокруг проблем, связанных с кишечником», пациенты стали более мобильными, активными, «успевали сделать намного больше из-за уменьшения/исчезновения проблем с кишечником», у них повысилась толерантность к физическим нагрузкам, больные стали менее раздражительными и более стрессоустойчивым. Наконец, в процессе лечения улучшилась социальная и личная жизнь пациентов, в том числе сексуальная.
Эффективность терапии сочеталась с высоким уровнем безопасности Колофорта. Отсутствие зарегистрированных в ходе исследования нежелательных явлений, имеющих достоверную связь с терапией, результаты повторной оценки показателей витальных функций пациентов и их лабораторных тестов позволили подтвердить безопасность препарата, которая была сопоставима с безопасностью плацебо. Следует отметить высокий уровень приверженности пациентов этой схеме лечения Колофортом (близкий к 100% по казатель комплаентности), низкий (менее запланированного) коэффициент выбывания пациентов в ходе исследования, в том числе по причине неэффективности терапии, отсутствие случаев несовместимости препарата с лекарственными средствами разных классов, применяемыми для лечения основной и сопутствующей патологии.
В ходе исследования показано, что Колофорт оказывает выраженный анальгетический эффект у пациентов со всеми вариантами СРК, это проявлялось в виде снижения интенсивности главного (первичного) симптома заболевания — абдоминальной боли. У 90% пациентов, ответивших на терапию Колофортом,значимое снижение тяжести абдоминальной боли регистрировалось более 50% длительности периода наблюдения. У 1/3 участников исследования болевой синдром полностью купировался к окончанию периода лечения. Анальгетический эффект развивался в течение первых 2 нед терапии и отмечался у 100% больных.На фоне лечения Колофортом не было зарегистрировано ухудшения или обострения заболевания.
Уменьшение выраженности болевого абдоминального синдрома и восстановление моторно-эвакуаторной функции ЖКТ на фоне лечения Колофортом происходило за счет воздействия на центральные и периферические звенья патогенеза СРК. Терапевтические эффекты препарата были обусловлены влиянием его компонентов (анти-ФНО-a, анти-S100 и анти-Н) на висцеральную гиперчувствительность и гипералгезию, субклинически выраженное воспаление и психофизиологические расстройства.
В результате лечения снижалась тяжесть и абдоминальной боли и другой гастроэнтерологической симптоматики, связанной с нарушенным транзитом кишечного содержимого, повышенным газообразованием и другими патологическими изменениями в кишечнике.Колофорт оказывал значимое положительное влияние на паттерн стула (форму и частоту) у пациентов с разными вариантами СРК. К окончанию 3 мес терапии из 96% больных подгруппы СРК с преобладанием диареи, ответивших на лечение, 1/2 пациентов имели нормальный тип стула; при этом его частота снизилась с 3 раз и более до 1–2 раз за сутки; у 100% больных с положительной динамикой формы стула по Бристольской шкале отмечалось значимое снижение интенсивности абдоминального болевого синдрома.
Средняя частота стула у пациентов подгруппы СРК с преобладанием запоров от исходных 1–2 раз в неделю увеличилась до 3–7 раз за 7 дней; одновременное улучшение паттерна стула и анальгетический эффект Колофорта зарегистрированы у 84% больных.
Все пациенты отмечали снижение выраженности «негастроэнтерологических» соматовегетативных и психофизиологических расстройств, повышение физической и умственной работоспособности, активности и стрессоустойчивости, уменьшение раздражительности и эмоциональной лабильности. Итогом позитивного влияния на разные стороны физического и психического здоровья было улучшение повседневной, общественной и личной, в том числе сексуальной, жизни пациента, т.е. качества жизни в целом.
Таким образом, результаты проведенного многоцентрового двойного слепого плацебо-контролируемого рандомизированного исследования свидетельствуют об эффективности и безопасности применения Колофорта в лечении больных с разными вариантами СРК. Рекомендуемая длительность лечения Колофортом должна составлять не менее 3 мес, а учитывая нарастающий в течение 12-недельного курса эффект, можно рекомендовать его продление до 6 мес.
Наверное, на планете Земля не найдется такого «счастливчика», который ни разу не произнес бы эту фразу. Причем – с полным на то основанием.
Читать полностью«Базовые» симптомы СРК – это боль и спазмы в животе, «усиленное» газообразование (метеоризм), диарея и запоры, способные «приходить на смену» друг другу, внезапные позывы к опорожнению кишечника и другие «неполадки в животе»
Читать полностью